気まぐれ解説カフェ(仮)
中学受験算数の入試問題を今日もゆるゆる解説中。算数プリントの無料ダウンロードは右横カテゴリ「プリントの無料ダウンロード」からどうぞ。
06/26
Sat
2010
洛星2010【2】 ☆濃度・食塩水のやり取り☆
濃度が13%の食塩水120gが入った容器Aと、7%の食塩水120gが入った容器Bがあります。容器Bから食塩水をいくらか容器Aに移したところ、容器Aの食塩水の濃度が11%になりました。
(1) 容器Bから容器Aに移した食塩水の量は何gですか。
そのあと、容器Aの食塩水から水を蒸発させてから40gを容器Bに移したところ、容器Bの食塩水の濃度が9%になりました。
(2) 容器Aから蒸発させた水の量は何gですか。
※ 続きを見る場合は、下の「解説はこちらから」をクリック!
(1)
次の図のように、容器Bから濃度7%の食塩水を□g取り出し、それを濃度13%の食塩水が120g入った容器Aに入れてよくかきまぜたら、容器Aの食塩水は濃度が11%になりました。
※ 画像はすべて、クリックすると拡大します。
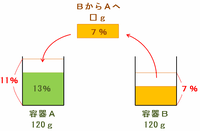
容器BからAへ移した食塩水の量を□gとおくと、容器Aの食塩水の濃度が11%になった様子は次のような天びん図に表すことができます。
上の図の支点の左側は11-7=4%、右側は13-11=2%なので、左右のうでの長さの比は左:右=4:2=2:1になります。
容器BからAへ移した食塩水の量を□gとおくと、容器Aの食塩水の濃度が11%になった様子は次のような天びん図に表すことができます。
上の図の支点の左側は11-7=4%、右側は13-11=2%なので、左右のうでの長さの比は左:右=4:2=2:1になります。
また、重さの比は長さの逆比なので、左:右=1:2になります。
上の図の120gが赤い比の②、そしてBからAへ移した食塩水の量(図の□g)は赤い比の①にあたるので、答えは120÷2=60gになります。
(2)
さっきの作業の結果、次の図1のように容器Bには濃度7%の食塩水が120-60=60g残り、容器Aには濃度11%の食塩水が120+60=180g入っています。
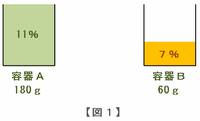
その後、次の図2のように容器Aを加熱すると水だけが蒸発するので、食塩水の濃度がアップします。
加熱する前の容器Aには食塩が180×0.11=19.8gふくまれていますが、加熱した後も食塩の量は変わらない(食塩は蒸発しない)ので、19.8gの食塩はそのまま残ります。
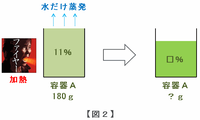
図2の作業で濃くなった容器Aの食塩水から40gを取り出し、今度はそれを次の図3のように容器Bへ入れてからよくかきまぜます。
図2の作業で濃くなった容器Aの食塩水から40gを取り出し、今度はそれを次の図3のように容器Bへ入れてからよくかきまぜます。
すると、容器Bの食塩水は濃度が7%から9%へと変化しました。
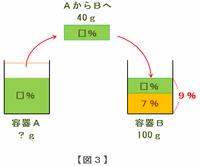
図3の容器Bで濃度が9%になった様子を天びん図に表すと次の図4のようになります。
下の図の重さの比は左:右=60g:40g=③:②なので、左右のうでの長さの比は左:右=②:③になります。
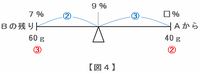
上の図の9-7=2%が青い比の②にあたるので、青い比の①は2%÷②=1%になります。
ここで容器Aの食塩水の濃度や重さの変化を振り返ってみると・・・
上の図の9-7=2%が青い比の②にあたるので、青い比の①は2%÷②=1%になります。
青い比の③は1%×③=3%なので、図の□には9+3=12%があてはまります。
ここで容器Aの食塩水の濃度や重さの変化を振り返ってみると・・・
① 最初は濃度13%の食塩水が120g入っていた。
② 容器Bの食塩水を70g混ぜたら濃度11%の食塩水が180gできた。
③ 容器Aを加熱したら水だけが蒸発して、濃度が12%になった。
④ ②と③のときにふくまれる食塩の量は、どちらも19.8gのままである。
という流れになっています。
PR
Comment
学校名で検索!
「フェリス」、「麻布」などの学校名を入力して検索すると該当記事の一覧が表示されます。 「該当なし」だったらごめんなさいm(_ _)m
カテゴリー
最新記事
(12/18)
(12/17)
(12/16)
(12/15)
(12/14)
(12/13)
(12/12)
(12/11)
(12/10)
(12/09)
(12/08)
(12/07)
(12/06)
(12/05)
(12/04)
(12/03)
(12/02)
(12/01)
(11/30)
(11/29)
リンク
最新コメント
プロフィール
HN:
ゆんたく
性別:
非公開
職業:
たびびと(Lv.4)
趣味:
チェロの演奏
自己紹介:
かつてゆんたくと呼ばれていたゆんたくです。
こんなゆんたくへ何か個人的に連絡したいことがおありでしたら、下記アドレスまでメールにてお願いいたします。
hassysar@gmail.com
こんなゆんたくへ何か個人的に連絡したいことがおありでしたら、下記アドレスまでメールにてお願いいたします。
hassysar@gmail.com
